


Propiedades físicas y químicas
-
Los alcanos que tienen entre 1 y 4 átomos de carbono son gases a temperatura ambiente. Por ejemplo: Metano (CH4), principal componente del gas natural.
-
Alcanos que tienen entre 5 y 17 átomos de carbono son líquidos a esa misma temperatura. Por ejemplo: Heptano (C7H16), componente de la gasolina.
-
Los alcanos que tienen 18 carbonos o más son sólidos a temperatura ambiente. Por ejemplo: Icosano (C20H42), presente en ceras y parafinas (para hacer velas).
Las propiedades físicas de los alcanos están en gran medida determinadas por el número de átomos de carbono que contienen en su estructura.
Propiedades físicas de los alcanos
Entre las propiedades están las siguientes:
-
Escasa solubilidad. En general, los alcanos son poco o nada solubles en agua y, a medida que aumenta el peso molecular, la solubilidad se torna incluso menor. En solventes orgánicos, sin embargo, la solubilidad es alta.
-
Baja densidad. Su densidad es menor que la del agua, por eso tienden a flotar. Esto se ve muy bien cuando se producen derrames de hidrocarburos en el mar, como por ejemplo, los derrames de petróleo (mezcla de muchos hidrocarburos). Por otro lado, la densidad de los alcanos aumenta a medida que aumenta su masa molecular, es decir, la cantidad de átomos de carbono.
-
Punto de fusión y ebullición variable. El punto de fusión y de ebullición dependen del número de átomos de carbono (a mayor número, más elevado es el punto de fusión y el de ebullición), pero también de la estructura: las estructuras lineales tienen un punto de fusión y ebullición más alto que las ramificadas. El punto de ebullición de los alcanos aumenta aproximadamente 30 °C cada vez que se agrega un átomo de carbono al compuesto.
-
Conductividad eléctrica. Por lo general, los alcanos no conducen la electricidad.




Solventes orgánicos
Agua
Gasolina
Derrame hidrocarburos en el océano



Propiedades químicas de los alcanos
Las reacciones más comunes que pueden sufrir los alcanos son:
-
Oxidación. Al combinarse con el oxígeno pueden formar dióxido de carbono y agua y liberar energía bajo la forma de calor. Esta es la típica reacción de combustión.
-
Halogenación. Tanto el cloro como el bromo, el flúor y el yodo pueden sustituir a átomos de hidrógeno del alcano. Los productos de reacción consisten en distintas proporciones de diferentes alcanos halogenados. Un ejemplo es el cloroformo, que es un hidrocarburo halogenado (el triclorometano).
-
Nitración. A altas temperaturas y en presencia de vapores de ácido nítrico, se puede producir la sustitución de un hidrógeno por el grupo NO2–, lo que genera nitroalcanos en distintas proporciones.
-
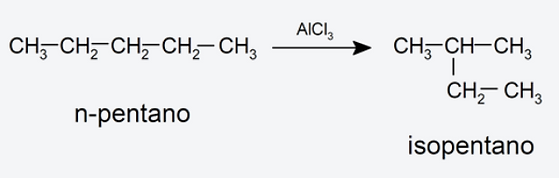
Isomerización. Es la reestructuración de la molécula sin pérdida ni ganancia de átomos. Por lo general, esta reacción requiere el uso de catalizadores. Por ejemplo:
-
Pirólisis. Es la descomposición de los alcanos por exposición a muy elevada temperatura y sin presencia de aire, de esta forma se evita su combustión y se prioriza la descomposición de las moléculas rompiendo sus enlaces químicos. Esta reacción se utiliza en la industria para obtener alquenos y alcanos de cadenas cortas a partir de alcanos de cadenas más largas.




ESCANEA EL CODIGO Y SIGUE APRENDIENDO
